上回說到�����,玻爾度完蜜月����,9月初回到了哥本哈根����,在一所不知名的技術學院謀得了一份差事,玻爾清楚他現(xiàn)在的主要任務�����,并不是給學生們上課��,而是要著手解決盧瑟福遺留下來的兩個問題:
第一�����,盧瑟福原子模型不穩(wěn)定,電子在繞原子核運行的時候會釋放出電磁輻射����,導致電子會瞬間墜入原子核。
第二���,盧瑟福沒有說��,電子在核外是怎樣排布的�,當然這時人們也不清楚元素化學性質的本質�����,更不知道元素周期表中的元素化學性質為啥會表現(xiàn)出周期性的規(guī)律�。
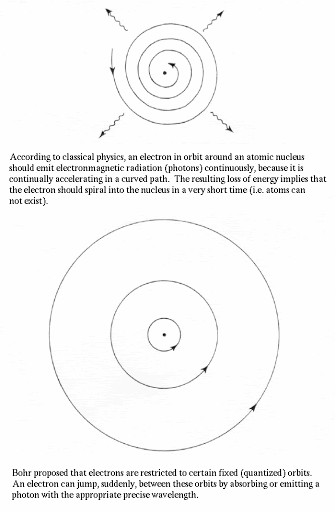
先說第一個問題,電子墜入原子核這是經(jīng)典力學和經(jīng)典電磁學預測出來的結果����,只要你相信經(jīng)典物理學在原子尺度上是正確的���,那么盧瑟福的原子必定坍塌�����。
那么玻爾是如何考慮這個問題的�?他必須在經(jīng)典物理學和盧瑟福原子模型之間做出選擇,很顯然他相信自己老師的模型是正確的���。
那玻爾就要回答為什么原子沒有坍塌��?玻爾認為����,這只能說明��,經(jīng)典物理學的某些結論在微觀尺度上并不適用����。
要想原子不坍縮,只能假設電子可以在某些特定的軌道運行�,在這些軌道上運行的電子,并不釋放輻射���。
這些軌道被稱為電子的穩(wěn)定態(tài)軌道�����。也就是說����,電子在核外的軌道并不像經(jīng)典物理學認為的那樣,可以在任意距離上繞核運行��,而是電子有特定軌道�,并不連續(xù)。

舉個容易理解的例子����,比方說,我們的太陽系只有太陽和地球�,地球繞太陽的軌道可以是任意的大小,地球距離太陽可以是0.8億公里����,可以是1億公里,可以是1.333億公里��,你能想到的任何數(shù)字都可以�。
但玻爾現(xiàn)在說,地球只能在距離太陽1億公里����、2億公里���、3億公里的軌道上運行����,除了這些允許的軌道之外,地球不能存在于任何軌道之上��。
對于電子來說也一樣�,它只能在特定的軌道上運行,在這些軌道上原子是穩(wěn)定的�,而不會坍塌。
這就是玻爾找到的第一條線索��,假設穩(wěn)定態(tài)軌道的存在�,或者說電子的軌道不連續(xù)。不過�����,玻爾很清楚��,這里存在一個循環(huán)論證的問題�,即:為什么電子存在穩(wěn)定態(tài)軌道,因為在這些軌道上電子不輻射能量�,那為什么電子在這些軌道上不輻射能量,因為這些軌道是穩(wěn)定態(tài)軌道��。
你看,這種循環(huán)論證很顯然沒有說服力�����,所以玻爾需要找到第二條線索來解釋�����,為什么電子的軌道不連續(xù)�����,電子在這些軌道上所具有的能量是多少�?以及各個穩(wěn)定態(tài)軌道的半徑是多少?
玻爾為了考慮這個問題�����,工作也不準備要了��,1912年的年底請了幾個月的假���,專門找了一個僻靜的鄉(xiāng)下思考這個問題�。
在圣誕節(jié)前夕,他無意中在約翰·尼科爾森的論文中發(fā)現(xiàn)了關鍵性的一點�,也是玻爾需要找到的第二條線索�����。
尼科爾森這個人��,玻爾并不陌生��,他在劍橋學習的時候見過這個人�����,當時并沒有給玻爾留下多少印象�,尼科爾森在自己的論文中論證了這樣一件事。
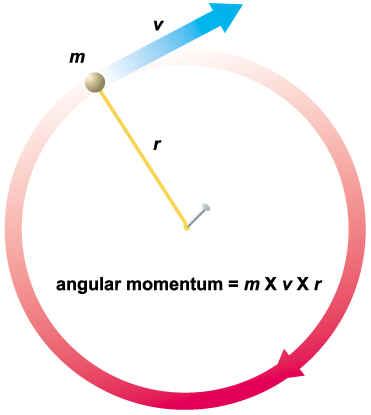
在經(jīng)典物理學中��,任何有質量的物體在運動的時候都有動量���,那動量怎么算����?質量乘以速度�����,一個做圓周運動的物體也有動量,不過他叫角動量����,角動量等于質量乘以半徑再乘以線速度。
經(jīng)典物理學對角動量的大小沒有做任何的限制���,也就是說角動量也是連續(xù)的�,但是尼科爾森發(fā)現(xiàn)�����,電子的角動量并不是連續(xù)的���。
它的角動量必須是h/2Π的整數(shù)倍����,h/2Π為角動量量子�����,是角動量的最小單位��,用h把表示,也叫約化普朗克常數(shù)����;
比如一個電子的角動量只能是1倍的h把,2倍的h把��,3倍的h把�,等等���,直到n倍的h把�。
這就是玻爾找到的第二條線索�,在這期間玻爾多次寫信告訴盧瑟福,他會盡快把原子論文交給他�����。盧瑟?����;匦耪f:不要給自己太大的壓力�。但玻爾清楚,他的同行現(xiàn)在也在研究原子模型�����,所以玻爾非常著急。
玻爾現(xiàn)在知道了為什么原子只能在特定的軌道上運行����,因為它的角動量是量子化的,所以它的軌道也是量子化的����。
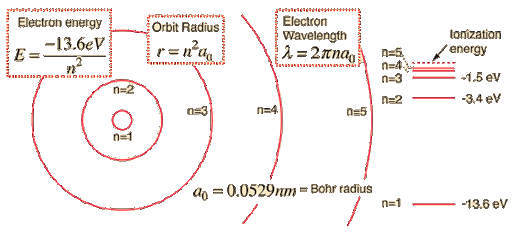
玻爾用字母n表示電子的軌道量子數(shù),n只能是正整數(shù)����,在每個軌道上電子都擁有自己特定的軌道能量,稱為能級����,用En表示。
玻爾以氫原子為例��,計算出了氫原子的各個電子軌道能級的大小��,以及軌道半徑的大小��,比如 n等于1的時候��,電子處在最低的能級,稱為基態(tài)����,能量為-13.6電子伏特,ev是能量單位���,表示一個電子在通過1伏特的電勢差之后����,所獲得的動能�����。
這個能量單位非常小�,專門是用來表示原子層面上的能量�����,我們?nèi)粘I钪胁粫褂玫诫娮臃?����,而是會用到焦耳���。原因是電子伏特太小�,寫起來很麻煩?
例如,1電子伏特等于1.602×10^-19焦耳���,每瓦等于每秒1焦耳��,生活中100瓦的燈泡釋放的能量如果用電子伏特表示的話���,可以寫成:6.24×10^20電子伏特/秒。這是一個天文數(shù)字�,足以見得電子伏特的大小。
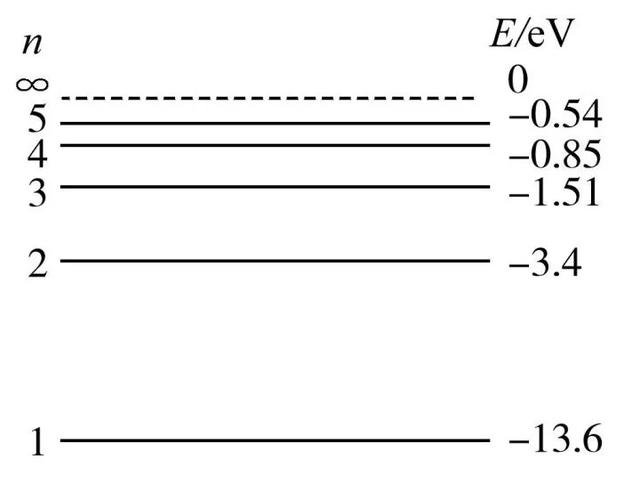
回到正題��,接著說原子��,基態(tài)的能量算出來了��,那其他能級的能量呢����?其他能級也叫激發(fā)態(tài),玻爾發(fā)現(xiàn)其他能級的能量等于基態(tài)的能量除以軌道量子數(shù)的平方����,即(E/n)�,比如n等于2時����,這個能級的軌道能量等于-13.6ev/4,結果是-3.4ev���。
玻爾還計算出電子處在基態(tài)時�����,氫原子的大小為5.3納米�����,其他能級的軌道半徑為基態(tài)的軌道半徑乘以n的平方。比如基態(tài)的軌道半徑為r�����,那么n等于2的軌道半徑就是4r����,以此類推為9r,16r����。
到現(xiàn)在為止����,玻爾已經(jīng)建立了一個量子化的原子模型���,但是一個正確的理論����,需要解釋一些以前人們無法解釋的現(xiàn)象����,不然這個理論就空有一副皮囊,毫無用處����。
所以玻爾還需要找到第三條線索,來完成自己的原子論文��,那么第三條線索在哪����?他的一位朋友漢斯·漢森,是玻爾在哥本哈根大學認知的����,這位朋友現(xiàn)在也從國外留學回來���,他留學的地方是德國的歌根廷大學,前面的視頻說過��,德國是光譜學研究的前沿陣地�����。
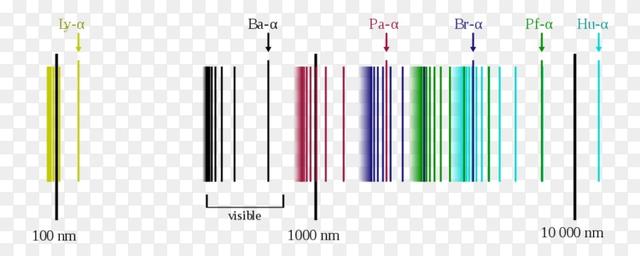
漢斯當然也掌握了不少的光譜學知識���,他問玻爾��,你的原子模型能不能解釋原子的發(fā)射光譜�����?他建議玻爾了解下氫原子光譜的巴爾末公式。關于原子的發(fā)射光譜我們在之前的視頻有詳細地說到�,這里就不重復了。
不過說到巴爾末公式�,我們還得把時間倒回到1850年,這一年物理學家安德斯詳細地測量了氫原子的的發(fā)射光譜����,在可見光中�����,氫原子有四條光譜線����,分別落在了紅光�����、綠光���、藍光�����、紫光的區(qū)域�,對應的波長為656.210�、486.072、434.01和410.12納米�����。
當時的人們就很好奇,你說這原子的光譜線是怎么來的��?為什么是分立的而不是連續(xù)的�?這兩個問題很難回答,是今天玻爾即將要解決的問題�����。
不過當時的人們還是做出了一個巨大的突破���,既然已經(jīng)測量出了氫原子在可見光中的四條光譜線的波長�,那么這些波長之間有什么關系����?能不能用一個數(shù)學公式來表示一下。
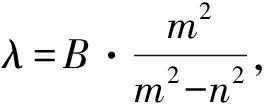
這就要提到一位瑞典中學的數(shù)學老師了��,他叫約翰·巴爾末�����,他經(jīng)常給朋友抱怨說�����,自己每天都過得都很無聊�����,也沒有啥數(shù)學難題困擾他�,他的朋友就告訴巴爾末,要不你來算算氫原子光譜線的波長之間有啥關系���,也就是上面那四個數(shù)字之間的關系���。
這位老爺子還真是牛,難怪他整天無聊�����,在1884年的6月巴爾末真就用一個公式把這四條光譜線表示了出來����。這個公式長這樣。
公式中m和n都是正整數(shù)����,b是常數(shù)�,值為364.56納米���。當我們讓n等于2的時候��,m分別取3�、4�����、5�、6,算出來的波長正好就是上面的四個數(shù)字����,還真的是神奇。這四條線現(xiàn)在也被稱為氫原子光譜的巴爾末系�����。
巴爾末老爺子就想���,這個n能不能是其他數(shù)呢���?比如n等于3�����,m取4、5��、6�����、7���,算出來的個波長又代表了什么���?
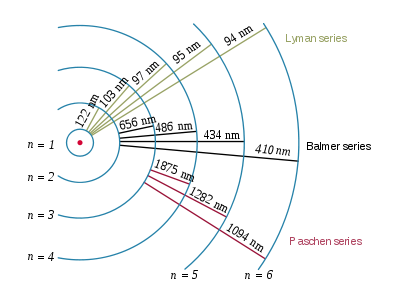
事實證明,巴爾末公式預測出了氫原子在紅外區(qū)域的發(fā)射光譜�,1908年這些光譜線被帕邢發(fā)現(xiàn),命名為帕邢系�����。
那n等于1呢��?m輪番取值���,又是啥���?這是氫原子的在紫外線區(qū)域的發(fā)射光譜��,現(xiàn)在叫萊曼系���。
不得不說,數(shù)學真的是神奇���,難怪人們說數(shù)學是大自然的語言��。巴爾末公式很成功地預言了氫原子的發(fā)射光譜�����,但是沒有一個人知道為什么這個公式這么管用��?沒人知道這其背后的物理學意義�。
當玻爾看到這個公式之后�,立馬知道了是咋回事。這不就是電子在不同能級之間躍遷嘛�。當n等于1,這就是基態(tài)���,m等于2���、3���、4��、5����、6,這些都是激發(fā)態(tài)�,每一個激發(fā)態(tài)的電子向基態(tài)躍遷都會以電磁波的形式釋放出兩個能級之間的能量差。波長可以用普朗克-愛因斯坦公式直接算出來�����。
至此���,玻爾完成了對盧瑟福原子的改造�����,量化原子模型�����,他量化了電子的角動量����,為原子模型加入了一個量子數(shù),可以叫它軌道量子數(shù)�,現(xiàn)在稱為主量子數(shù),用n表示�����。
1913年的3月玻爾把論文的第一部分給了盧瑟福�����,你可能會覺得奇怪��,這時的玻爾已經(jīng)完全獨立了����,為什么要先交給盧瑟福,而不是直接發(fā)表�。
原因很簡單,玻爾雖然獨立,但畢竟還很年輕����,如果能有一位德高望重的人物給論文寫個寄語啥的,可以提高影響力����,也能讓論文快速得到發(fā)表。
其次也是最重要的一點���,玻爾真的很敬重自己的老師���,盡然曾經(jīng)盧瑟福的猶豫不決導致了玻爾錯失了一項發(fā)現(xiàn)����,但在玻爾心里盧瑟福對他的評價依舊很重要。

盧瑟福在看了論文以后��,還真的提出了不少批評的意見�,比如玻爾說的電子躍遷,從一個軌道閃現(xiàn)到另外一個軌道���,就像王者榮耀里的閃現(xiàn)技能����,讓盧瑟福覺得像撞了鬼一樣,無法接受�����。
還有�����,假如電子現(xiàn)在處在了第三激發(fā)態(tài)����,他可以像第二軌道和基態(tài)躍遷,那么電子如何選擇它向哪個軌道躍遷��?
假如它躍遷到了第二激發(fā)態(tài)��,那么為什么電子選擇了第二激發(fā)態(tài)而不直接選擇基態(tài)��?假如電子直接躍遷到了基態(tài)���,它為什么不選擇先去第二激發(fā)態(tài)����?
在盧瑟福看來�����,電子好像有自由意志一樣���,說白了就是違反了因果律����,你看�,從玻爾這里人們的世界觀就開始出現(xiàn)了裂痕,不過盧瑟福想到這也沒多想�,也沒多為難玻爾,因為玻爾也拿不出答案���。
就在1916年的時候,愛因斯坦也發(fā)現(xiàn)了電子躍遷時候違反了因果律��,需要用概率去解釋它躍遷的時間�����,以及躍遷的能級����,愛因斯坦第一次把概率引入了量子論���,他還專門寫信給波恩說,自己接受不了自己發(fā)現(xiàn)的概率解釋?����,F(xiàn)在看來�����,愛因斯坦挺有趣的�,自己推動了量子論的發(fā)展,最后自己卻接受不了�����。這件事���,后面的視頻我們會再次提到����。
盧瑟福除了以上兩點接受不了以外��,他還嫌棄玻爾把論文寫得太長了,要求縮減篇幅�����。玻爾這次是死磕到底����,說啥都不會改自己的論文,一個符號都不行�����。
可能是玻爾上次吃了虧���,這次長記性了��,不停地盧瑟福寫信�,還專門跑到曼徹斯特找盧瑟福���,待在老師家里不走,盧瑟福這次被玻爾搞的精疲力盡���,最后做出了讓步��,同意玻爾發(fā)表論文���。

1913年的7月�、9月�����、11月���,玻爾的三篇論文一字未改的發(fā)表在了《哲學雜志》上����,史稱“三部曲”�����。

在往后的10年間����,玻爾利用自己的原子模型去解釋元素周期表的問題,也就是開頭我提到的第二個問題�。
而在這10年間,年輕的小伙子們���,泡利���、海森堡���、狄拉克正在成長,他們的學習生涯中聽得最多的就是玻爾的原子理論對原子光譜���,以及元素周期表的解釋�����,都獎玻爾視為自己的偶像���。
不過,玻爾的原子模型發(fā)表以后并沒有立即獲得人們的認可�,他還需要兩個實驗的驗證。這是我們下個視頻的內(nèi)容�。
從這以后,我們就真正地涉足了量子世界���,你會發(fā)現(xiàn)很多不可思議的現(xiàn)象����。
(本文內(nèi)容來源于李論科學�����,如有侵權聯(lián)系刪除?���。?/strong>